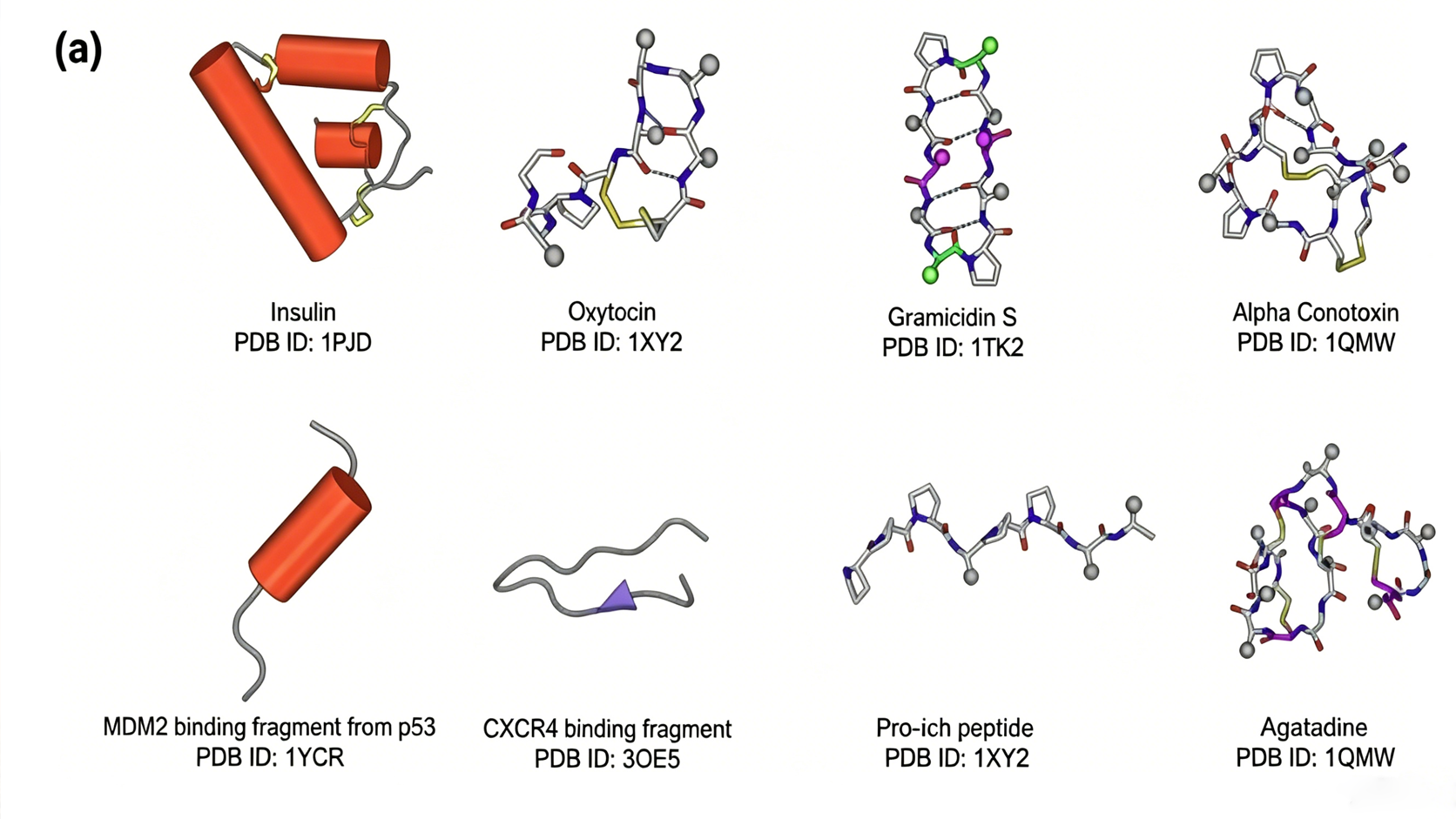
현대 약리학의 풍경에서 펩타이드 약물 발견은 고위험 분야로 부상했습니다. 소분자와 생물학적 의약품 사이의 "중간지대"로 설명되는 펩타이드는 이전에 "약물화 불가능"으로 간주되었던 표적을 다루기에 독특한 위치에 있습니다.
최근 생성 AI와 구조 생물학 모델의 폭발적인 증가로 AI 기반 펩타이드 설계는 실험실의 호기심에서 제약 R&D의 초석으로 이동하고 있습니다. 이는 펩타이드가 다음 AI "브레이크아웃" 히트가 되는 이유에 대한 심층 분석입니다.
01 | 골드ilocks 분자: 왜 펩타이드인가?
펩타이드 약물 발견의 기본 논리는 그들의 독특한 물리적 및 화학적 성질에 있습니다.
- 격차 해소: 소분자 약물은 깊은 "주머니"가 없어 큰, 얕은 단백질-단백질 상호작용(PPI) 인터페이스에 결합할 수 없는 경우가 많습니다.
- 세포내 공간 표적화: 항체(생물학적 의약품)는 표면 단백질을 식별하는 데 뛰어나지만, 크기가 크기 때문에 세포막을 통과하여 세포내 표적에 도달할 수 없습니다.
- 펩타이드의 장점: 펩타이드는 높은 특이성과 친화력을 유지하면서 단백질 표면에 적응할 충분한 유연성을 가지고 있습니다. 이는 세포내 PPI 표적을 열기 위한 이상적인 "열쇠"를 만듭니다.
- 검증된 트랙 레코드: 펩타이드 요법은 새로운 것이 아닙니다—인슐린부터 100개 이상의 FDA 승인 펩타이드 약물까지—but AI는 이제 이 분야를 고속 개발 단계로 가속화하고 있습니다.
02 | 데이터 장벽: 양보다 질
AI 세계에서 첫 번째 장애물은 모델이 아니라 데이터 기반입니다. 펩타이드 설계는 고품질 구조 데이터의 부족으로 인해 일반적인 단백질 설계와 크게 다릅니다.
- 구조적 부족: ProPedia, PepBDB, CPSet과 같은 데이터베이스는 훈련의 기반을 제공하지만, 중복 샘플, 짧은 펩타이드 또는 구식 웹 호스팅으로 인해 문제가 많습니다.
- 혁신적인 데이터 소싱: 선도 연구자들은 이제 단백질 루프 영역을 "유사 펩타이드" 자원으로 취급하고 있습니다. 루프는 구조적 및 동적 방식으로 펩타이드 행동을 모방하기 때문에 펩타이드의 형태 공간을 채우는 중요한 참고 자료로 작용합니다.
- 하이브리드 미래: 펩타이드 설계의 미래는 "실제 실험 구조 + 가상 예측 구조(AlphaFold DB에서) + 서열 지식"을 통합하는 데 달려 있습니다.
03 | 예측에서 설계로: AI 역량의 세 가지 수준
이 분야에서 AI의 진화는 복잡성 증가의 명확한 궤적을 따릅니다.
수준 1: 상호작용 예측
단백질 표면이 펩타이드를 결합할 수 있는 위치와 중요한 잔기를 식별하는 것입니다. PepNN, CAMP, MaSIF와 같은 모델은 단백질 구조, 서열 및 표면 기하학을 통합하여 결합이 "발생하는지 여부와 위치"를 예측합니다.
수준 2: 복합 구조 예측
"여부"를 넘어 "방법"으로 이동합니다. 전통적인 도킹은 고유연성 펩타이드에서 어려움을 겪었지만, AlphaFold 3, RoseTTAFold All-Atom, Chai-1, Boltz-1과 같은 새로운 세대 모델은 다성분 모델링을 혁신했습니다. 그러나 비천연 및 거대고리 펩타이드에 대한 체계적인 벤치마킹은 여전히 과제입니다.
수준 3: 표적 특이적 설계
이것이 현재 "핫 존"입니다. AI는 더 이상 분석만 하는 것이 아니라 특정 표적에 결합하기 위해 처음부터 새로운 분자를 생성하고 있습니다.
04 | De Novo 펩타이드 설계를 위한 세 가지 생성 경로
이 리뷰는 현재 결합제의 de novo 설계에서 지배력을争夺하는 세 가지 주요 AI 경로를 강조합니다.
4.1 환각 기반 설계: 반복 최적화
이 "역 생성" 논리는 구조 예측 모델을 사용하여 무작위 서열이 원하는 표적 형태로 접히는지 판단합니다.
- EvoBind & EvoBind2: 이 모델들은 미리 알려진 결합 부위를 필요로 하지 않습니다. EvoBind2는 거대고리 펩타이드의 경우 75%, 선형 펩타이드의 경우 46%의 히트율을 보고했으며, 친화력은 마이크로몰에서 서브나노몰 수준까지 다양합니다.
4.2 서열-구조 공동 설계: 확산 혁명
이 방법들은 생성 중에 구조와 서열이 함께 진화하도록 허용합니다.
- DiffPepBuilder: SE(3)-등변 확산을 기반으로 하며, 단백질 언어 모델 임베딩과 비틀림 각도를 통합합니다.
- PepFlow: 흐름 매칭 기술을 사용하여 기하학 및 에너지 지표에서 고품질 다양성을 제공합니다.
4.3 서열 기반 방법: "불규칙" 표적 설계
전사 인자와 같은 많은 고가치 표적은 안정적인 구조가 없거나 매우 불규칙합니다. 이 경우 단백질 언어 모델(pLMs)이 우수한 선택입니다.
- PepMLM: 이 모델은 단백질 서열의 끝에서 "마스크 채우기"를 사용하여 결합제를 생성하며, 38% 이상의 히트율을 보고합니다.
- Cut & CLIP: 이는 "결합"에서 "분해"로 이동하며, 대조 학습을 사용하여 E3 리가제 매개 분해를 유발하는 펩타이드를 설계합니다.
결론: 왜 지금인가?
AI가 "예측 보조자"에서 "생성 화학자"로 전환하는 것은 전환점을 마킵니다. 구조 기하학과 서열 기반 언어 논리를 결합함으로써 AI는 마침내 펩타이드의 형태 복잡성을 해결하고 있습니다. 약물 발견을 위해 이는 세포의 "약물화 불가능"한 내부를 표적화하는 더 빠르고 정확한 경로를 의미합니다.

Copyright © 2026 上海吉尔多肽有限公司 Ltd. All Rights Reserved. POWERED BY WEIMOBTRADE